WODA
Właściwości chemiczne i fizyczne wody i jej budowa
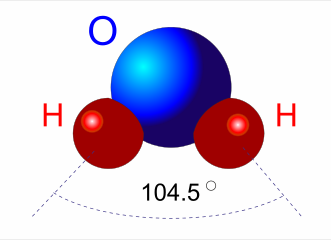
Zbudowana jest z dwóch atomów wodoru oraz jednego atomu tlenu połączonych wiązaniami kowalencyjnymi spolaryzowanymi. Wiązania kowalencyjne powstają między dwoma NIEMETALAMI, a powstałe wiązanie jest bardzo silne. Czemu spolaryzowane? Bo mamy tu różnice elektroujemności. Znaczy to, że pierwiastek bardziej elektroujemny przyciąga mocniej elektrony, niż ten mniej elektroujemny.
Mówi się, że cząsteczka wody ma budowę polarną i jest dipolem, ale co to właściwie znaczy? Żeby dobrze rozumieć właściwości wody trzeba zaprzyjaźnić się z jej chemicznymi właściwościami.
Elektroujemność jest to siła z jaką jeden z pierwiastków (w tym przypadku tlen) przyciąga elektrony od drugiego pierwiastka w związku chemicznym. (Trochę jak żona, która zawłaszcza pieniądze męża mówiąć: to wspólne kochanie, ale lepiej, żebym to ja sie nimi zaopiekowała 😉 ) dzięki temu nasze wiązanie staje się spolaryzowane. To znaczy że ładunek naszego wiązania jest rozłożony nierównomiernie– tlen jest bardziej ujemny bo przyjął elektrony, a wodór bardziej dodatni bo oddał. Cząsteczka z nierównomiernie rozłożonym ładunkiem ma dwa bieguny -czyli jest dipolem.
Dzięki temu, że cząsteczka jest dipolem posiada elektryczny moment dipolowy, a co za tym idzie możemy śmiało stwierdzić że ma budowę polarną.
WAŻNE: POLARNE ZWIĄZKI ROZPUSZCZAJĄ SIĘ W POLARNYM, A NIEPOLARNE ZWIĄZKI W NIEPOLARNYM. DLATEGO WŁAŚNIE WODA JEST ŚWIETNYM ROZPUSZCZALNIKIEM DLA WIELU CZĄSTECZEK O BUDOWIE POLARNEJ.
Dzięki temu, że woda jest dipolem może tworzyć wiązania wodorowe. Dzieje się tak ponieważ obdarowany elektronami tlen ma teraz ich “nadmiar” i jego wiązanie z wodorem zostało osłabione. W wyniku tego osłabienia może powstać wiązanie wodorowe pomiędzy silnie elektroujemną cząsteczką tlenu, a wodorem pochodzącym z innej cząsteczki.
Wiązania wodorowe są stosunkowo słabymi oddziaływaniami, jednak powstaje ich bardzo dużo. To powoduje, że żeby je wszystkie zerwać potrzeba dużej ilości energii!
- Duże napięcie powierzchniowe.
Jeśli wylejecie na stół kropelki wody, nie rozleją się one płasko na stole jak kleksy z atramentu na kartce, tylko stworzą małe wypukłe kropelki. Dzieje się tak, ponieważ między cząsteczkami wody działają siły kohezji czyli tzw. siły spójności. Cząsteczki wody się KOCHAJĄ i wolą silniej trzymać się siebie nawzajem niż cząsteczek “obcych”.
Siły adhezji (ADD– dodajemy nowe cząsteczki obok) to siły przylegania czyli w tym wypadku przylegania powietrza oraz wody.
W napięciu powierzchniowym siły kohezji są dużo większe niż siły ahdezji. Dzięki temu na powierzchni wody tworzy się niewidoczna “błona”, która może posłużyć nartnikom jako ułatwienie do poruszania się po jej powierzchni.
- Maksymalna gęstość w temperaturze 4 stopnie, większa gęstość wody w stanie ciekłym niż w stanie stałym.
Wzór na gęstość jest to [gestosc]= M/V
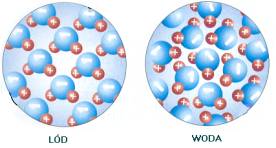
Dzięki temu, że woda jest dipolem cząsteczki oddziaływują ze sobą. Woda zamarzając przyjmuje przez to budowę krystaliczną- odległość między jej cząsteczkami zwiększa się pomimo niezmienionej masy. Skoro odległości się zwiększą to jej objętość wzrośnie. Pamiętając wzór łatwo jest nam określić, że skoro zwiększa się objętość czyli dzielnik, gęstość czyli nasz wynik musi zmaleć 🙂
Dzięki tym właściwościom woda w zimę o największej gęstości -> jest najcięższa i opada na dno. Największa gęstość przypada na 4 stopnie, więc ryby i inne stworzenia wodne będą w stanie przeżyć zimę przy dnie. Dodatkowo nasz lód, który jest ze wszystkiego najlżejszy, bo ma najmniejszą gęstość -> unosi się na powierzchni wody, tworząc warstwę izolacyjną. Dzięki temu niższe partie wody są chronione przed zamarznięciem.
- Wysokie ciepło właściwe
Czyli ilość ciepła, którą trzeba dostarczyć do jednostkowej masy, żeby spowodować jednostkową zmianę temperatury. Czyli np. trzeba dostarczyć x ciepła, żeby podnieść 1kg o 1 stopień. Dzięki temu, że woda jest dipolem i może tworzyć wiązania wodorowe jej ciepło parowania rośnie. Im więcej wiązań wodorowych powstanie, tym więcej energii trzeba włożyć, żeby je rozerwać. Ta właściwość jest bardzo ważna dla nas, ponieważ jest wykorzystywana w procesie termoregulacji.
Gdy jest nam gorąco, pocimy się aby uchronić nasz organizm przed przegrzaniem. Nasz pot w głównej mierze Na+, Cl+ oraz Woda. Ciepło z naszego organizmu jest oddawane na zewnątrz i “zużywane przez pot” na rozerwanie wiązań wodorowych i wyparowanie.
Jest to również bardzo ważne np. podczas wiosny, gdy rozpuszcza się lód po zimie. Nie następuje to szybko i gwałtownie, co mogłoby grozić np. powodzią, a powoli i długotrwale.
Znaczenie biologiczne wody
- Stanowi rozpuszczalnik związków ustrojowych – osocze stanowi aż 55% krwi, a 96% osocza to właśnie woda!
- Uczestniczy w wielu reakcjach metabolicznych np. jest niezbędna do zajścia cyklu Krebsa
- Stanowi środowisko życia dla wielu organizmów
- Niezbędny element diety
- Niezbędna do zachodzenia cykli roślin ewolucyjnie starszych np. paprotników lub mszaków